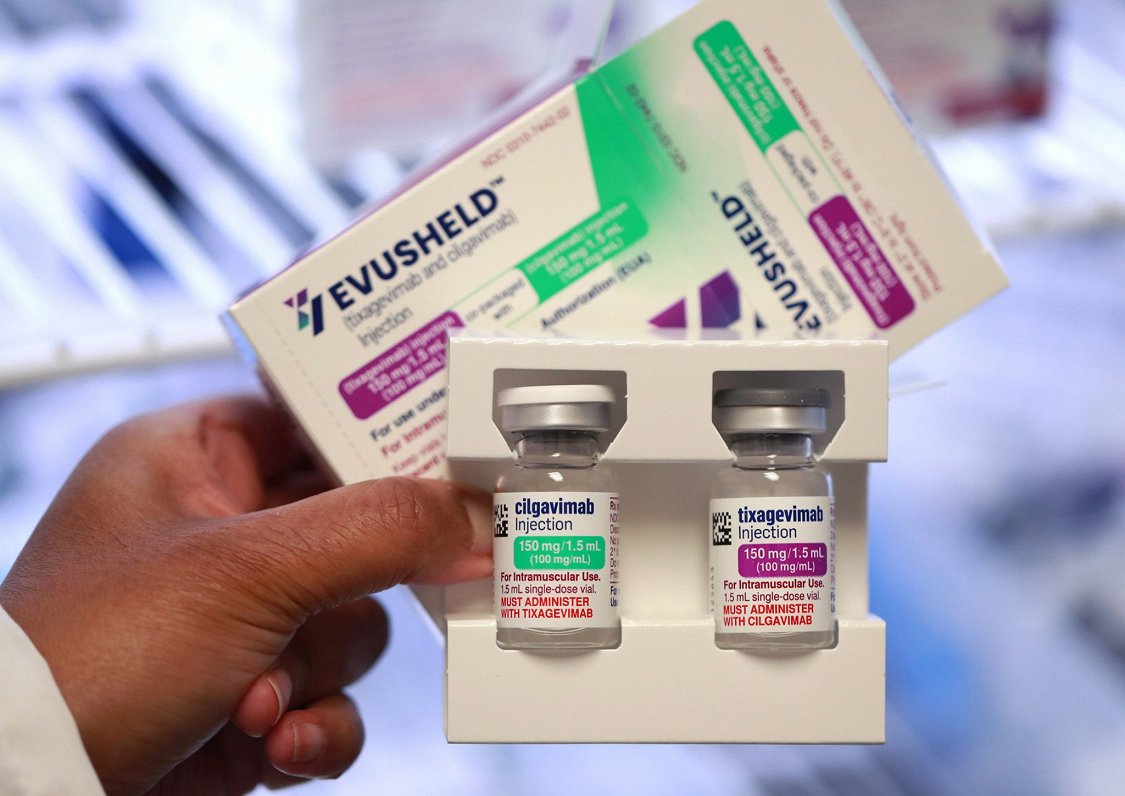
"Evusheld" satur divas aktīvās vielas – tiksagevimabu un cilgavimabu, divas monoklonālās antivielas, kas izveidotas, lai saistītos ar Covid-19 izraisošā SARS-CoV-2 vīrusa pīķa proteīnu divās dažādās vietās. Kad "Evusheld" antivielas saistās ar pīķa proteīnu, vīruss nespēj iekļūt šūnās, lai vairotos, un nespēj izraisīt Covid-19 infekciju.
ZVA skaidroja, ka šī lēmuma pieņemšanai CHMP izvērtēja datus no pētījuma, kurā piedalījās vairāk nekā 5000 personu un kas liecina, ka "Evusheld", ievadot divu injekciju veidā (150 mg tiksagevimaba un 150 mg cilgavimaba), samazināja Covid-19 infekcijas risku par 77%, aplēstajai aizsardzībai pret vīrusa infekciju ilgstot vismaz sešus mēnešus.
Pētījuma ietvaros pieaugušie, kuriem nekad nebija bijusi Covid-19 infekcija un kuri nebija saņēmuši Covid-19 vakcīnu vai citu profilaktisku līdzekli, saņēma "Evusheld" vai placebo jeb imitētu zāļu injekciju.
Pirmo sešu mēnešu laikā pēc "Evusheld" saņemšanas 0,2% personu (8 no 3441) tika laboratoriski apstiprināta Covid-19 infekcija, salīdzinot ar 1,0% personu (17 no 1731) placebo grupā.
"Evusheld" drošuma profils ir labvēlīgs un blakusparādības kopumā bija vieglas – neliels cilvēku skaits ziņoja par reakcijām injekcijas vietā vai hipersensitivitāti.
CHMP secināja, ka šo zāļu sniegtie ieguvumi atsver to riskus, lietojot tās apstiprinātajām indikācijām, un pārsūtīs savu ieteikumu Eiropas Komisijai visās ES dalībvalstīs piemērojama lēmuma pieņemšanai.
ZVA norādīja, ka
pētījuma dati tika apkopoti pirms vīrusa omikrona varianta parādīšanās, kas tagad nosaka Covid-19 infekcijas izplatību visā pasaulē.
Laboratoriskie pētījumi liecina, ka vīrusa omikrona BA.1 paveids varētu būt mazāk jutīgs pret tiksagevimibu un cilgavimabu 150 mg lielā devā nekā omikrona BA.2 paveids. EZA tuvākajās nedēļās izvērtēs datus, lai novērtētu, vai jauno vīrusa paveidu izraisītas Covid-19 infekcijas novēršanai varētu būt piemērotas citas zāļu devas.